創業時から続く私たちの遺伝子
Ingenuity in action

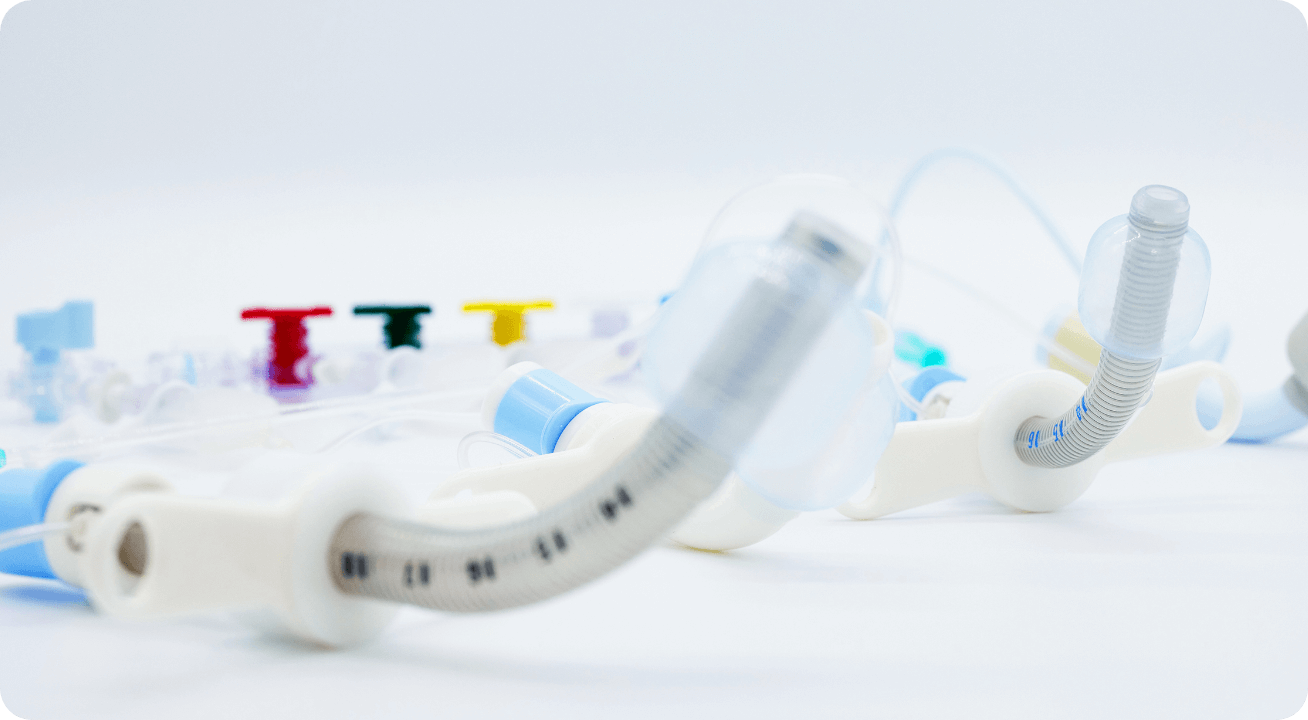
カテーテルをはじめとするシリコーン製医療機器の研究・開発・製造を進めてきた富士システムズ。その創業時から受け継がれ続けている遺伝子であるIngenuity in actionに込められた想いについてご紹介します。




シリコーンとともに生きる
シリコーンが持つ独自の特性に着目し、その可能性を広げようと立ち上がった私たち。創業時から今に至るまで、さまざまな研究・開発に携わってきました。
その中で培ってきた私たちの知見や開発力についてご紹介します。
製品関連情報




富士システムズについてもっと知る
新着情報
-
2023. 1. 24会社情報大阪支店が移転・稼働開始
-
2022. 3. 1会社情報関西物流センターを開設
-
2021. 10. 1会社情報